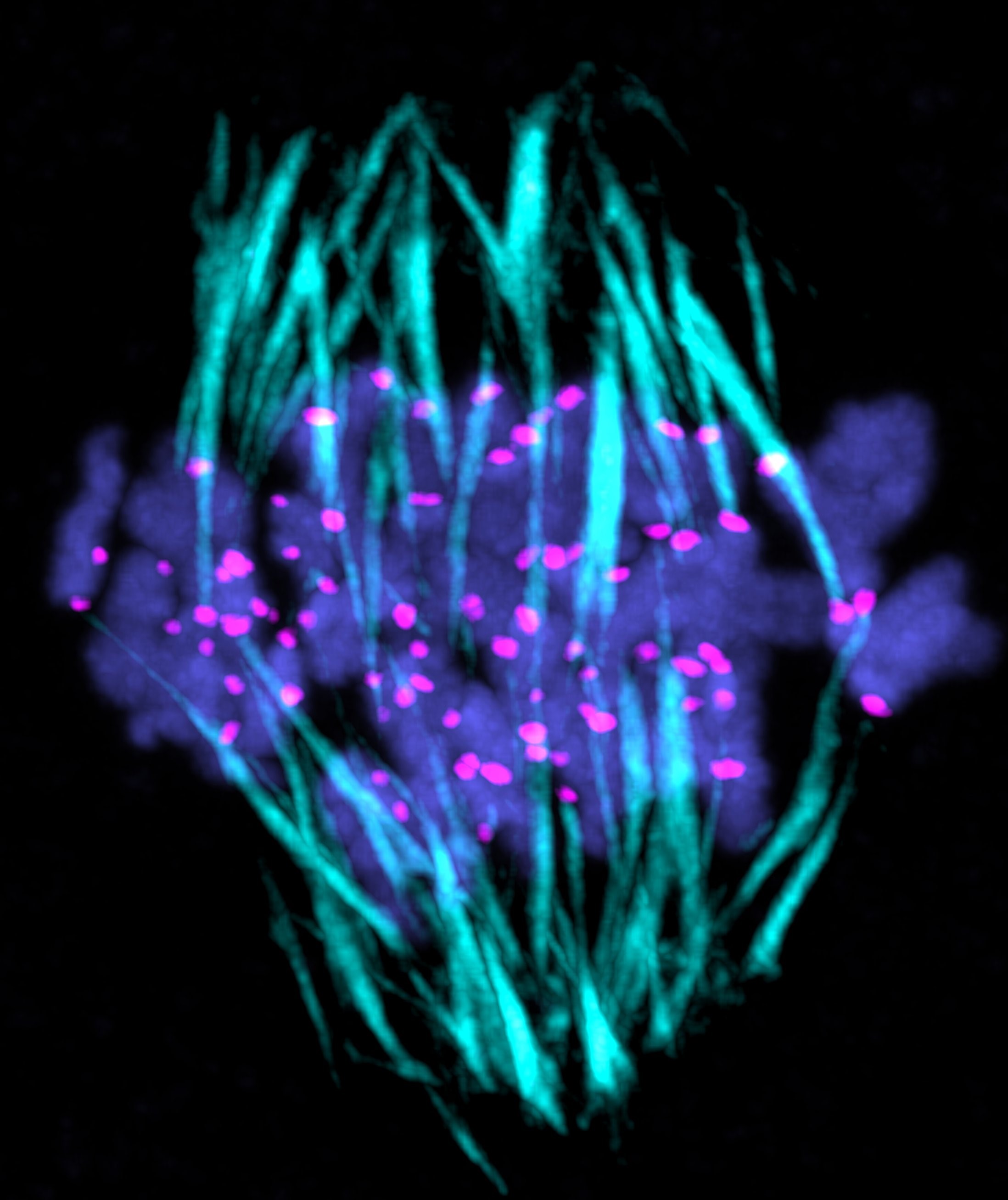
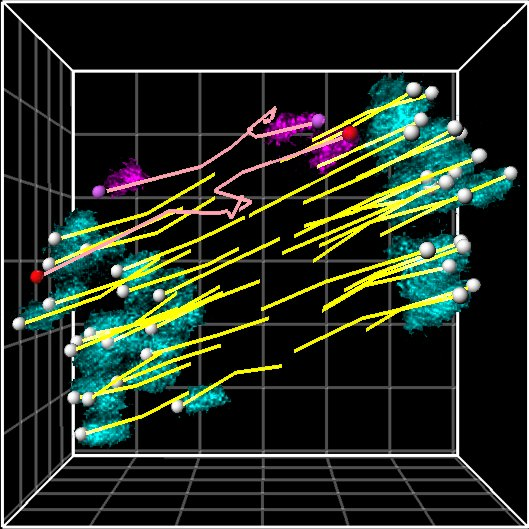
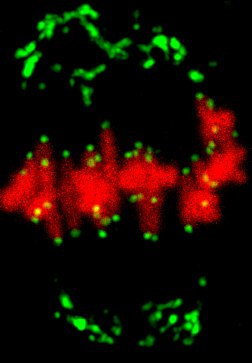
卵母細胞は減数分裂を行うことで卵子となります。卵子は受精して細胞分裂を繰り返すことで、やがて個体となります。私たちの研究室では、マウス卵のハイスループットかつ高解像度ライブイメージング技術、顕微操作技術、遺伝学的手法を組み合わせることで、卵母細胞の減数分裂と受精卵の体細胞分裂における染色体分配を研究しています。卵母細胞が行う最初の分裂が減数第一分裂です。このときの染色体分配はエラーが多く、その頻度は母体年齢とともに上昇します。続いて受精時に減数第二分裂が、受精後にはDNA複製を経て体細胞分裂が行われ、それぞれで染色体が分配されます。私たちは、これら3回の連続した細胞分裂における、異なる染色体分配のロジックを明らかにしていきます。卵母細胞の減数第一分裂における染色体分配の機構を明らかにし、なぜこの分裂で特にエラーが多く、しかも年齢とともにその頻度が上昇するのかを理解します。続く減数第二分裂、体細胞分裂のそれぞれの機構と比較することで、細胞が染色体分配の戦略を柔軟に使い分ける様を見出していきます。これらの研究から得られた成果を、さらに生殖医療分野との共同研究に活かしていきます。
研究テーマ
- 哺乳類卵母細胞の減数分裂における染色体分配機構の解析
- 受精卵の細胞分裂における染色体分配機構の解析
- 卵母細胞および受精卵における老化にともなうエラー
主要論文
Asai K, Zhou Y, Takenouchi O, et al.
Artificial kinetochore beads establish a biorientation-like state in the spindle.
Science
385(6715), 1366-1375 (2024)
doi: 10.1126/science.adn5428
Takahashi S, Kyogoku H, Hayakawa T, et al.
Embryonic genome instability upon DNA replication timing program emergence.
Nature
633, 686-694 (2024)
doi: 10.1038/s41586-024-07841-y
Takenouchi O, Sakakibara Y, Kitajima TS.
Live chromosome identifying and tracking reveals size-based spatial pathway of meiotic errors in oocytes.
Science
385(6706), (2024)
doi: 10.1126/science.adn5529
Mishina T, Tabata N, Hayashi T, et al.
Single-oocyte transcriptome analysis reveals aging-associated effects influenced by life stage and calorie restriction.
Aging Cell
20(8), e13428 (2021)
doi: 10.1111/acel.13428
Courtois A, Yoshida S, Takenouchi O, et al.
Stable kinetochore-microtubule attachments restrict MTOC position and spindle elongation in oocytes.
EMBO Reports
22(4), e51400 (2021)
doi: 10.15252/embr.202051400
Yoshida S, Nishiyama S, Lister L, et al.
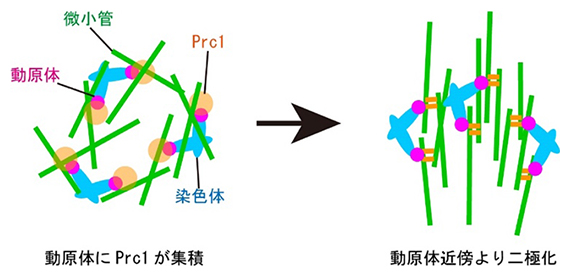
Prc1-rich kinetochores are required for error-free acentrosomal spindle bipolarization during meiosis I in mouse oocytes.
Nature Communications
11, 2652 (2020)
doi: 10.1038/s41467-020-16488-y
Ding Y, Kaido M, Llano E, et al.
The post-anaphase SUMO pathway ensures the maintenance of centromeric cohesion through meiosis I-II transition in mammalian oocytes.
Current Biology
28(10), 1661-1669 (2018)
doi: 10.1016/j.cub.2018.04.019
Kyogoku H, Kitajima TS.
Large cytoplasm is linked to the error-prone nature of oocytes.
Developmental Cell
41(3), 287-298 (2017)
doi: 10.1016/j.devcel.2017.04.009
Sakakibara Y, Hashimoto S, Nakaoka Y, et al.
Bivalent separation into univalents precedes age-related meiosis I errors in oocytes.
Nature Communications
6, 7550 (2015)
doi: 10.1038/ncomms8550
Yoshida S, Kaito M, Kitajima TS.
Inherent instability of correct kinetochore-microtubule attachments during meiosis I in oocytes.
Developmental Cell
33(5), 589-602 (2015)
doi: 10.1016/j.devcel.2015.04.020
メンバー
北島 智也
チームディレクター
吉田 周平
技師
島本 走
基礎科学特別研究員
越口 愛美
特別研究員
伏井 実穂子
特別研究員
京極 博久
客員研究員
濱田 香
テクニカルスタッフⅡ
浅井 皓平
研究パートタイマーⅠ
ZHOU Yuanzhuo
大学院生リサーチ・アソシエイト
向瀬 メイ明子
大学院生リサーチ・アソシエイト
金村 麗美
大学院生リサーチ・アソシエイト
佐久間 海帆
研修生
市原 笑美子
研修生
TANTRY Angela Jennifer
研修生
ニュース

2025年11月11日 BDRニュース
北島 智也 チームディレクターが「大阪科学賞」を受賞

2025年11月4日 研究成果
老化卵子の染色体数異常を抑止することに成功

2025年8月20日 研究成果
卵子の染色体は外側ほど気難しい

2025年6月9日 研究成果
卵子染色体の正常性維持におけるヒストン修飾の新たな役割を解明
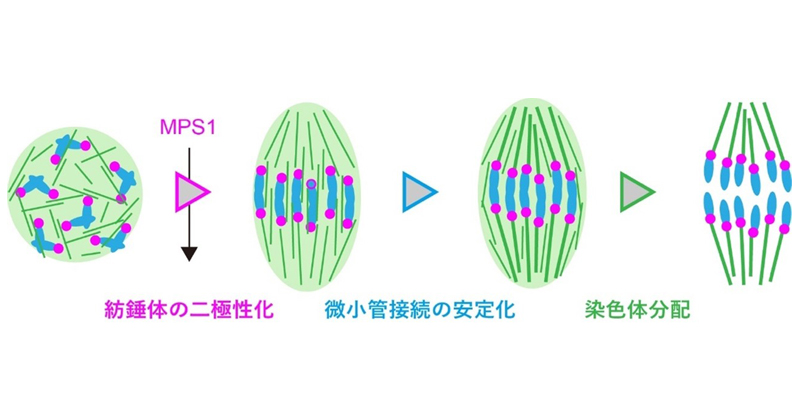
2025年6月4日 研究成果
卵子へ染色体を正しく分配する手順

2025年3月14日 BDRニュース
理研栄峰賞、理研梅峰賞、理研桜舞賞の授与について

2025年1月15日 BDRニュース
中学生が聞きました!
研究者への道のり〜竹之内 修さんの場合〜

2024年9月24日 研究成果
ゲノム解析から探る「幻の怪魚」アカメの進化と生存の歴史
2024年9月20日 研究成果
常識外れの新設計!世界初の人工動原体ビーズ
2024年8月29日 研究成果
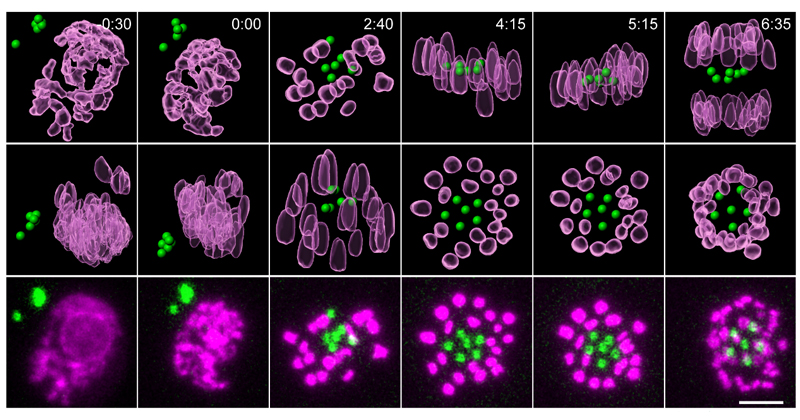
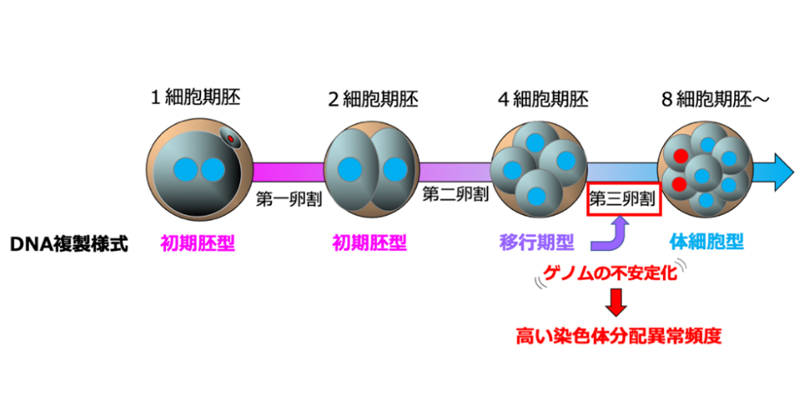
マウス初期胚の型破りなDNA複製様式を発見
2024年7月19日 研究成果
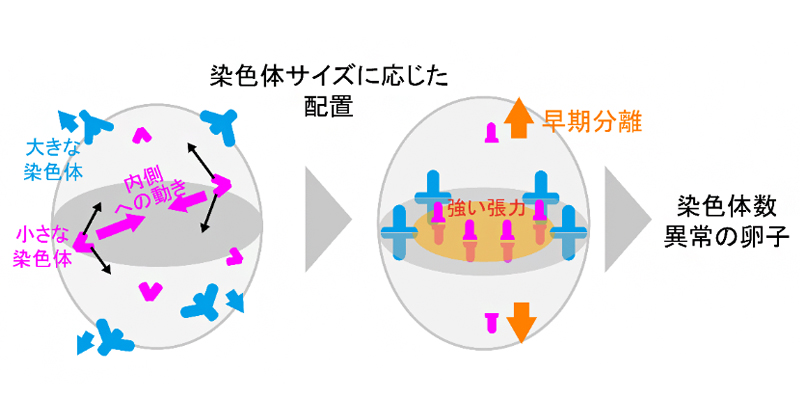
卵子の老化で小さな染色体が正しく分配されない原因
2023年10月20日 研究成果
カマキリを操るハリガネムシ遺伝子の驚くべき由来

2022年12月19日 BDRニュース
北島智也チームリーダーら理研の研究者4名が「日本学術振興会賞」を受賞

2022年10月21日 研究成果
天然記念物ヒブナの起源を解明
2022年5月19日 研究成果
無精子症マウスから産子獲得に成功
2021年9月2日 研究成果
精子DNAを捨てないで
2021年7月13日 研究成果
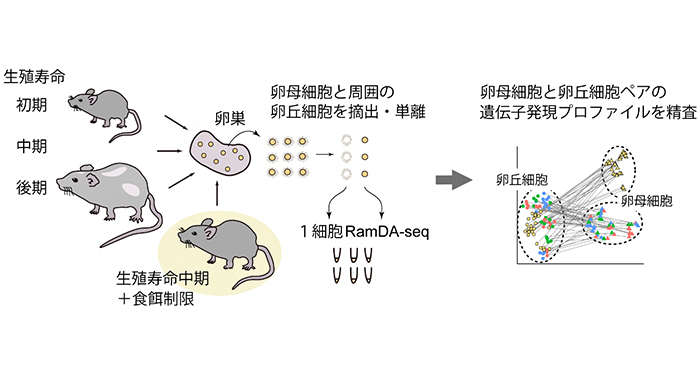
卵母細胞の老化を1細胞で捉える
2021年3月4日 研究成果
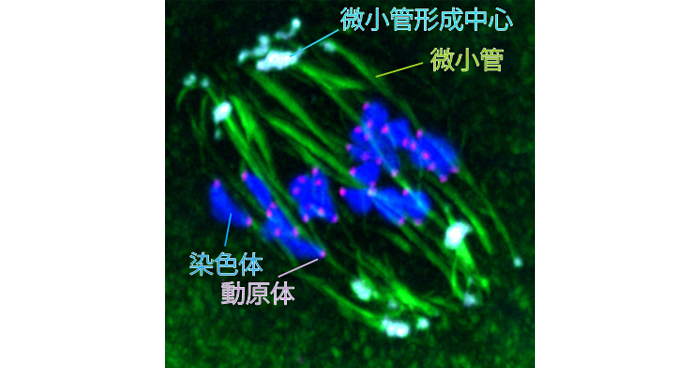
卵子のための染色体分配装置の調整

2020年12月17日 研究成果
卵子をかたち作る遺伝子群を同定

2020年11月4日 BDRニュース
BDRの研究ネホリハホリ
どうしてオスとメスがいるんだろう?
2020年5月27日 研究成果
卵母細胞における染色体分配装置の形成機構を解明

2019年11月27日 BDRニュース
研究者にズームイン
卵の研究でドイツand日本!

2019年1月19日 BDRニュース
京極博久 基礎科学特別研究員(染色体分配研究チーム)のエッセイが産経新聞の連載「科学の中身」に掲載されました
2018年6月12日 BDRニュース
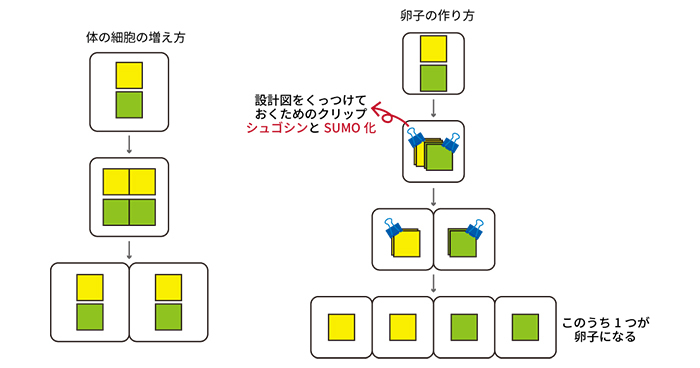
論文ノート
「シュゴシン」と「SUMO化」で卵子を守る!
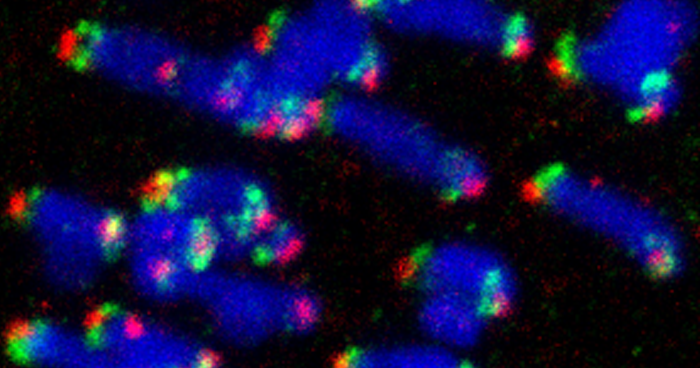
2018年5月11日 研究成果
卵子の染色体を守る新たな仕組み