上皮の折り曲げを引き起こすシグナルのリレー
2018年7月9日
体の中の臓器は、それぞれ特徴的な形をしている。例えば、眼球は球状の、中枢神経は筒状の構造をもつが、それらは全て平坦な一層のシート状の上皮組織が折れ曲がることによって形成される。ショウジョウバエの気管形成では、上皮組織の気管原基が体の内側に向かって陥入する事で作られる。この陥入に必要な細胞外シグナル調節キナーゼ(ERK)の活性は、気管原基の中心部から周辺部に向かって伝搬する事が知られているが、ERK活性伝搬の仕組みはわかっていなかった。
理研BDRの小椋陽介基礎科学特別研究員(形態形成シグナル研究チーム、林茂生チームリーダー)らは、ERK活性のライブモニタリングとシミュレーションを組み合わせて、ショウジョウバエ胚の気管原基の陥入時に必要なERKシグナルの活性化機構は、隣接する細胞に次々と伝搬していくリレーモデルによって説明できることを明らかにした。本成果は科学誌Developmental Cellに2018年7月16日付で掲載されるのに先立ち、2018年7月6日にオンラインで公開された。
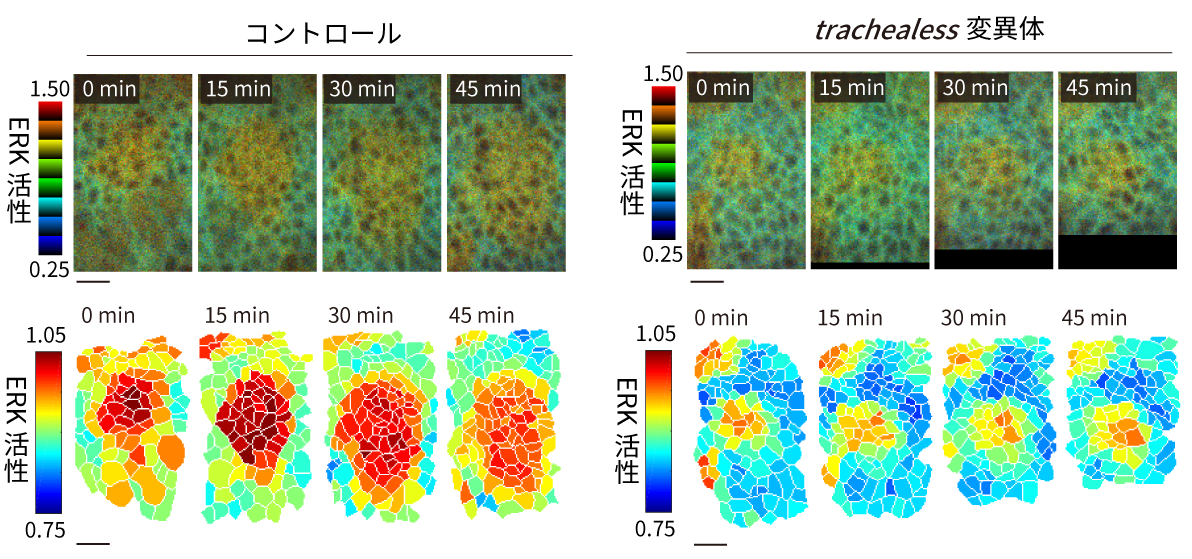
気管原基におけるERK活性化のシグナルが伝搬する様子。野生型(左)では中心部から周辺部に向かってシグナルが伝搬するが、trachealessを欠損させる(右)とシグナルは伝搬しない。
細胞の増殖や分化、運動性などに重要な役割を果たす細胞外シグナル調節キナーゼ(ERK)の活性化機構については、ERKの活性勾配によってシグナルが伝搬されるとするモデルと、個々の細胞のスイッチのリレーによってシグナルが伝搬されるとするモデルが提唱されている。ショウジョウバエ胚の気管原基が陥入するときにはERKの活性化が必要であり、このERK活性化には上皮成長因子受容体(EGFR)からのシグナル伝達が必要である。EGFRシグナル伝達は、上皮成長因子(EGF)様リガンドの一種であるSpitz(Spi)が結合することによって活性化される。Spiは不活性型の前駆体として細胞内で合成され、ゴルジ体の膜上でエンドペプチターゼRhomboidによって切断されて活性化し、活性型Spiは細胞外に分泌されてEGFRのリガンドとなる。したがって、Rhomboid発現細胞はEGFRのリガンドを産生する細胞であると考えて差し支えない。ERKの活性化が伝搬する細胞境界には、EGFR-ERKシグナルに依存してミオシン繊維が蓄積し、陥入を促進する張力が発生する。では、この気管原基の陥入に必要なERK活性の伝搬は、ERKの活性勾配モデルあるいはリレーモデルのどちらで説明することができるのだろうか。
ショウジョウバエの胚発生の過程で起こる気管原基の陥入におけるERK活性化の時間的変化を可視化するために、小椋らは蛍光共鳴エネルギー移動を利用した蛍光プローブを用いてERK活性化のタイムラプスイメージングを行った。その結果、ERKの活性化は気管原基の中心部の細胞から段階的に周辺部の細胞へと広がって行くことがわかった。また、ERKの活性化を引き起こすRhomboidの発現も、ERK活性化と同時に起こった。したがって、気管原基が陥入するときのERK活性化は、オンとオフがスイッチのように切り替えられることによってシグナルが伝搬するリレーモデルによって説明できることが示唆された。
では、気管原基の陥入に必要なERKの活性化を制御しているスイッチとはなんなのだろうか。小椋らは、ERKの活性化に必要なRhomboidに注目した。気管原基におけるRhomboidの発現に必須の転写因子Trachealess を欠損させたショウジョウバエ胚においてERKの活性化についてFRETを用いて観察したところ、ERK活性の伝搬は観察されなかった。またEGFRを欠損させたショウジョウバエ胚でも同様にERK活性の伝搬は観察されなかった。つまり、ERK活性化にはRhomboidによるSpiの活性化と、細胞外に分泌されたSpiが自己細胞の、あるいは隣接細胞のEGFRに結合することが必要であり、このEGFRシグナルの下流でまたRhomboidの発現が誘導されることでERK活性が正のフィードバック制御を受けることが示唆された。また、このシグナル伝達によってショウジョウバエ胚の気管原基が陥入するのに必要なミオシン繊維の収縮パターンが決められることがわかった。
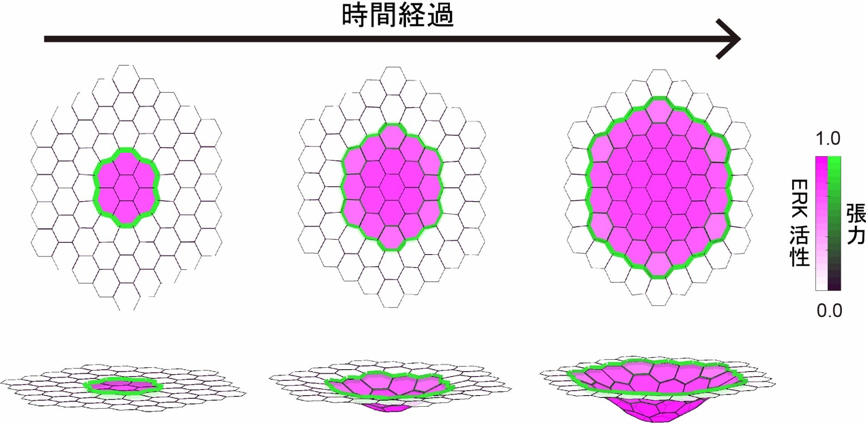
ERK活性化のシグナルリレーモデルによって陥入が起こることを示すシミュレーション図。細胞ごとのERK活性の強さを紫色の勾配で、細胞境界で発生するミオシン繊維による張力の大きさを緑色の勾配で示す。
ここまでの観察から導かれるERK活性化のリレーモデルは、力学的に妥当なのだろうか。このことを検討するため、RhomboidによるERK活性化のスイッチ切り替えとリレーモデルによるシグナルの伝搬によって陥入が起こる数理モデルを作成し、シミュレーションを行った。SpiとERKの活性化が中心部分の細胞に限局している状態からシミュレーションを行うと、ミオシン繊維はERKが活性化している細胞の外側の境界に集積した。また、ERKの活性化が中心から3列目の細胞に到達したときに陥入が始まり、4列目になるとその深さが深くなったが、これはショウジョウバエ胚で観察される陥入の進行とよく似ていた。
「生きているショウジョウバエ胚を観察し、そこから導き出された正のフィードバック制御機構を持つリレーモデルが、気管原基の陥入時に必要なERK活性化の伝搬に最適であることを証明できました。」と林チームリーダーは語る。「リレーモデルによると、伝搬の過程でERK活性は減衰しませんが、これのような波はトリガー波と呼ばれます。トリガー波の減衰しない性質は、サイズの異なる器官を同じ仕組みで作るためのシグナル伝達の巧妙な仕組みだと考えられます。ショウジョウバエや今回開発した数理モデルを用いてシグナルの伝搬について理解することは、将来的には臓器を望みのサイズで形成させる再生医療の基盤技術につながる可能性を秘めています。」
高橋 涼香(BDR・広報グループ)
関連リンク
掲載された論文
関連記事





