チームリーダー
崔 翼龍
Ph.D.
生体機能動態イメージング研究チーム
[2023年3月 終了]
E-mail cuiyl[at]riken.jp
[at]を@に変えてください
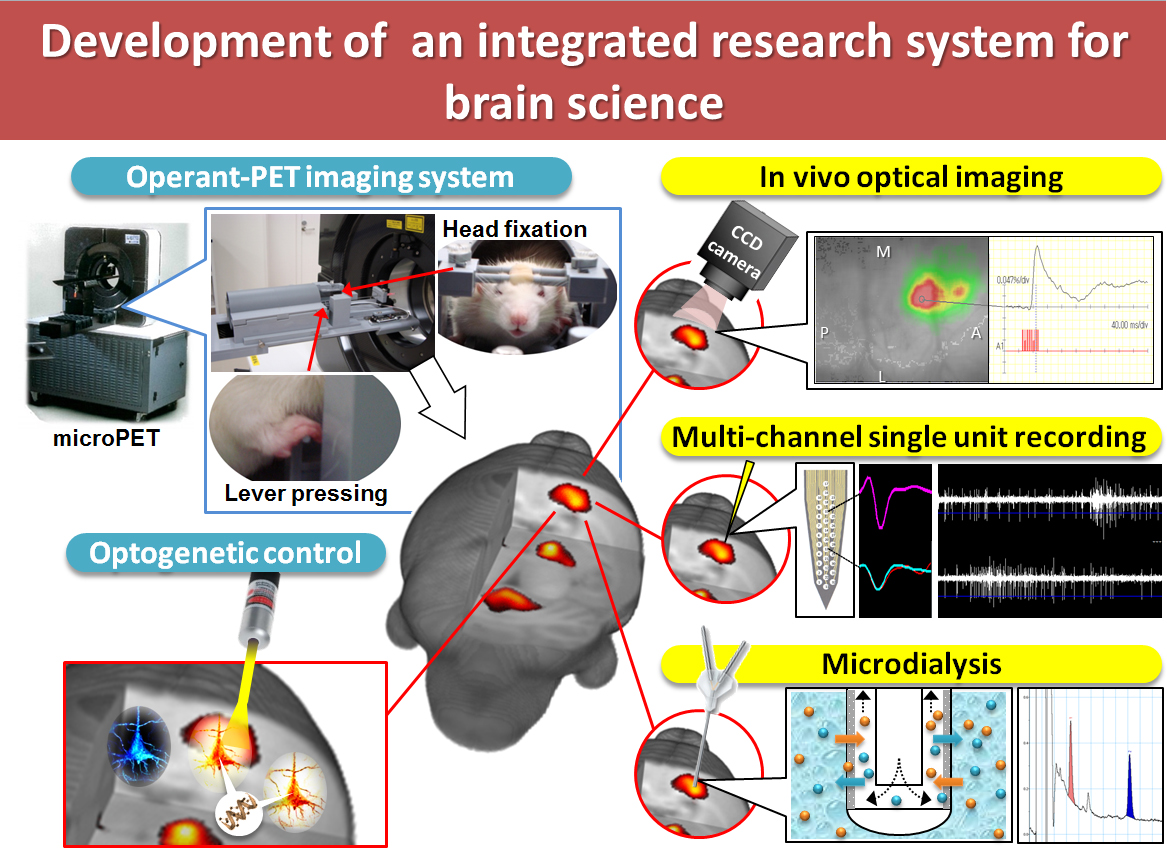
生命は長年の進化を経て、生体機能に最適化した内部環境を獲得しており、生体内の機能分子は多階層性の複雑な内部環境の中で、周辺の微小環境と巧みに作用し合って、安定した内部環境を維持しています。 安定した内部環境からの逸脱は、生体機能分子の時・空間的なダイナミクスを乱し、個体の機能低下や疾患の発症を引き起こすと考えられます。我々は分子の振る舞いを生きた生体内で定量評価できるPETイメージングを基軸として、さらに神経生理学・機能解剖学・行動薬理学・遺伝子工学などの手法と組み合わせ、個体の機能低下や疾患に関わる機能分子の振る舞いを統合的に理解することを目指して研究を進めています。特に、疾患の前段階であり、発症を未然に防ぐことが可能な亜健康状態での機能分子の振る舞いやこころによる機能分子のダイナミックな変化を捉え、その神経生物学基盤の解明を目指しています。
研究テーマ
- PETイメージングを基軸とした統合的な脳研究システムの構築および精神神経活動の神経生物学的基盤の解明
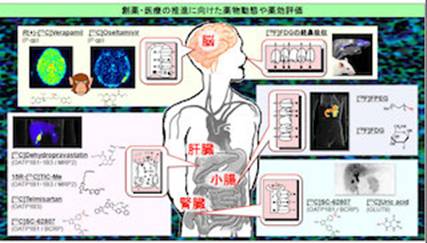
- PETイメージングを活用した薬物動態研究
- がん特異的なPETイメージング法の開発および新規診断・治療薬の評価
主要論文
Hu D, Li D, Shigeta M, et al.
Alleviation of the chronic stress response attributed to the antioxidant and anti-inflammatory effects of electrolyzed hydrogen water.
Biochemical and Biophysical Research Communications
535, 1-5 (2021)
doi: 10.1016/j.bbrc.2020.12.035
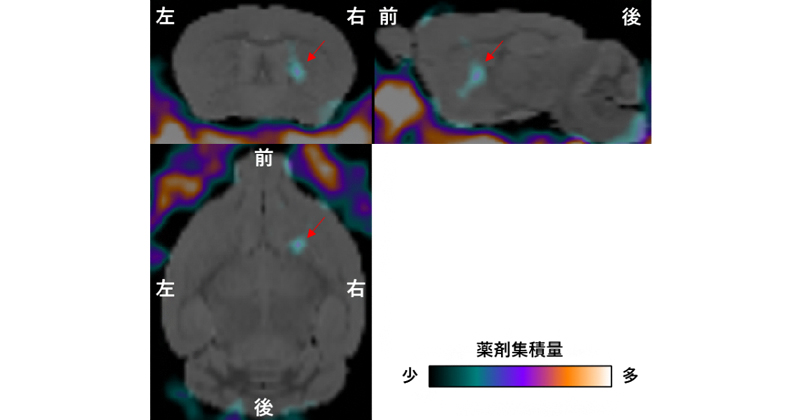
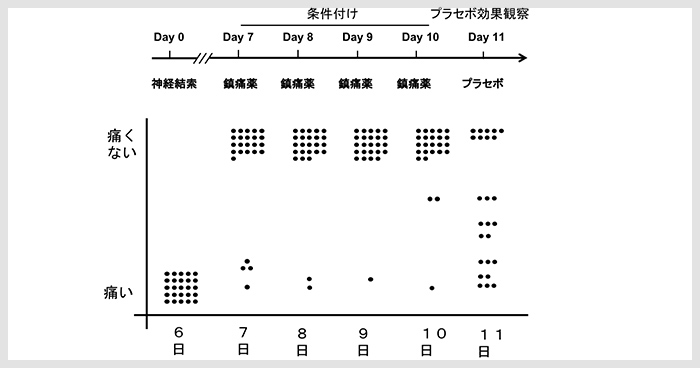
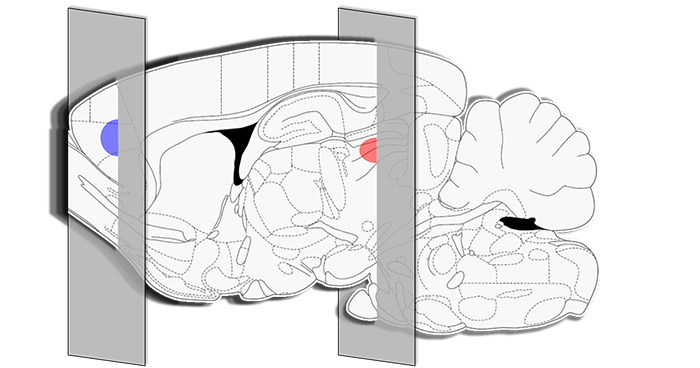
Zeng Y, Hu D, Yang W, et al.
A voxel-based analysis of neurobiological mechanisms in placebo analgesia in rats.
NeuroImage
178, 602-612 (2018)
doi: 10.1016/j.neuroimage.2018.06.009
Fujita S, Mizoguchi N, Aoki R, et al.
Cytoarchitecture-dependent decrease in propagation velocity of cortical spreading depression in the rat insular cortex revealed by optical imaging.
Cerebral Cortex
26(4), 1580-1589 (2016)
doi: 10.1093/cercor/bhu336
Kanzaki A, Okauchi T, Hu D, et al.
Extension of recovery time from fatigue by repeated rest with short-term sleep during continuous fatigue load: Development of chronic fatigue model.
Journal of Neuroscience Research
94(5), 424-429 (2016)
doi: 10.1002/jnr.23718
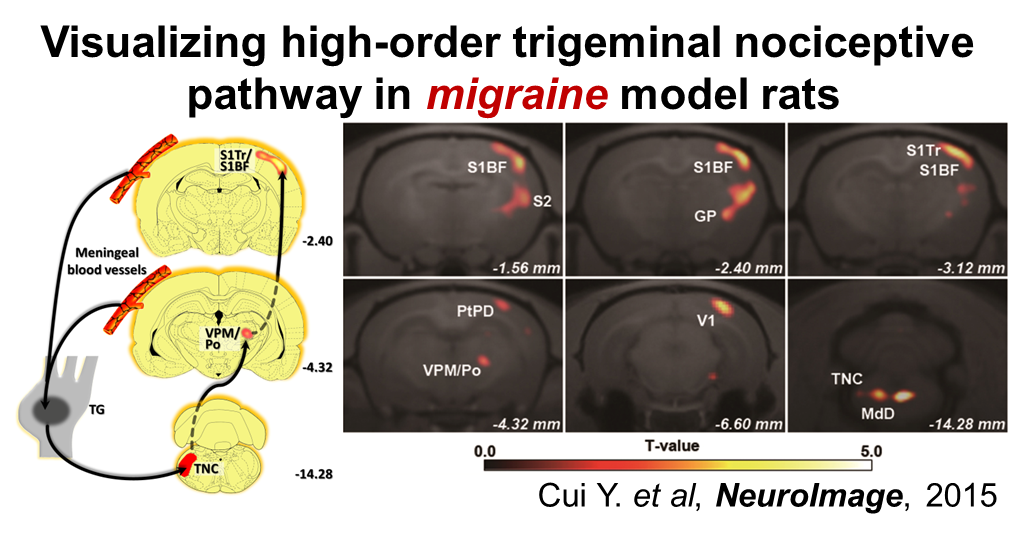
Cui YL, Toyoda H, Sako T, et al.
A voxel-based analysis of brain activity in high-order trigeminal pathway in the rat induced by cortical spreading depression.
NeuroImage
108, 17-22 (2015)
doi: 10.1016/j.neuroimage.2014.12.047
Mukai H, Ozaki D, Cui Y, et al.
Quantitative evaluation of the improvement in the pharmacokinetics of a nucleic acid drug delivery system by dynamic PET imaging with F-18-incorporated oligodeoxynucleotides.
Journal of Controlled Release
180, 92-99 (2014)
doi: 10.1016/j.jconrel.2014.02.014
Sako T, Hasegawa K, Nishimura M, et al.
Positron emission tomography study on pancreatic somatostatin receptors in normal and diabetic rats with 68Ga-DOTA-octreotide: a potential PET tracer for beta cell mass measurement.
Biochemical and biophysical research communications
442(1-2), 79-84 (2013)
doi: 10.1016/j.bbrc.2013.11.001
Shingaki T, Takashima T, Ijuin R, et al.
Evaluation of Oatp and Mrp2 Activities in Hepatobiliary Excretion Using Newly Developed Positron Emission Tomography Tracer [C-11]Dehydropravastatin in Rats.
Journal of Pharmacology and Experimental Therapeutics
347(1), 193-202 (2013)
doi: 10.1124/jpet.113.206425
Takashima T, Nagata H, Nakae T, et al.
Positron emission tomography studies using (15R)-16-m-[11 C]tolyl-17,18,19,20-tetranorisocarbacyclin methyl ester for the evaluation of hepatobiliary transport.
Journal of Pharmacology and Experimental Therapeutics
335(2), 314-323 (2010)
doi: 10.1124/jpet.110.170092
Akazawa KH, Cui YL, Tanaka M, et al.
Mapping of regional brain activation in response to fatigue-load and recovery in rats with c-Fos immunohistochemistry.
Neuroscience Research
66(4), 372-379 (2010)
doi: 10.1016/j.neures.2009.12.009
Cui YL, Takashima T, Takashima-Hirano M, et al.
11 C-PK11195 PET for the in vivo evaluation of neuroinflammation in the rat brain after cortical spreading depression.
Journal of Nuclear Medicine
50(11), 1904-1911 (2009)
doi: 10.2967/jnumed.109.066498
Cui YL, Takamatsu H, Kakiuchi T, et al.
Neuroprotection by a central nervous system-type prostacyclin receptor ligand demonstrated in monkeys subjected to middle cerebral artery occlusion and reperfusion: a positron emission tomography study.
Stroke
37(11), 2830-2836 (2006)
doi: 10.1161/01.STR.0000245088.60282.22
メンバー
HU Di
研究員
根山 広行
研究員
WU YuPing
テクニカルスタッフⅠ
井上 美智子
テクニカルスタッフⅠ
重田 美香
テクニカルスタッフⅠ
越智 祐太
テクニカルスタッフⅠ
植田 尚子
アシスタント