分化せずに自己複製するのは難しいが、恒常性維持のためには重要だ
2021年3月5日
身体の中にはさまざまな幹細胞がいるが、骨髄の中にはあらゆる血液細胞を作り出す「造血幹細胞」がいる。いると言ってもその数は非常に少なく、骨髄内の有核細胞の10万個に1個程度と非常に少ない。そのごくわずかな造血幹細胞が、身体中で働く数千億以上の白血球や赤血球、血小板などを毎日作り出している。細胞を増やすためには細胞分裂をしなければならないし、多種多様な細胞を作りだすためには幹細胞からそれぞれの細胞に分化していかなければならない。しかし、細胞分裂でできた2つの細胞が両方とも分化してしまったら、造血幹細胞が骨髄内から消えてしまう。そのため、造血幹細胞は細胞分裂時に、分化するための細胞と造血幹細胞で居続ける細胞に分裂すると予想される。しかし、そのメカニズムがどのように維持され、破綻するのか、その詳細はよく分かっていない。
理研BDRの酒巻太郎大学院生リサーチ・アソシエイト(臨床橋渡しプログラム造血幹細胞開発研究、宮西正憲研究リーダー)らは、長期造血幹細胞と短期造血幹細胞と呼ばれる細胞群を各々分離し解析するという独自の実験手法を用いることで、造血幹細胞の自己複製能が細胞分裂というストレスの程度により柔軟に変化すること、さらにはその過程にHoxb5が強く関与していることを明らかにした。本成果は科学誌 Biochemical and Biophysical Research Communicationsに2021年2月5日付で掲載された。
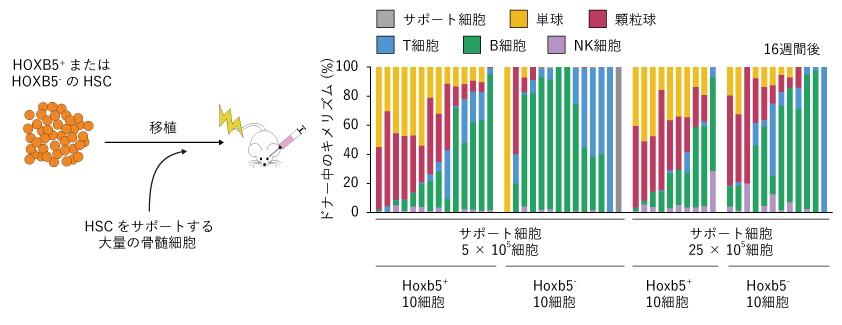
図1.HSCと同時に大量の骨髄細胞を移植すると、Hoxb5-のST-HSCからも長期的に
ターンオーバーの短い単球や顆粒球が作り出されており、自己複製能を維持していることが分かる。
幹細胞は、自分と同じ特徴を持つ幹細胞に分裂できる「自己複製能」と様々な細胞に分化できる「多分化能」の両方を有する細胞と一般的に定義づけられている。幹細胞は細胞分裂を繰り返しながら身体を構成するさまざまな細胞に分化し、各組織、臓器の恒常性を維持する。この過程において、造血幹細胞は自己複製能を多分化能よりも先に失うと考えられている。しかしながら、自己複製能が失われると、細胞分化に伴い幹細胞の数が減少し、結果的に造血不全に至る。そのため、幹細胞の自己複製能がどのように維持され、破綻するのか、その制御機能を理解することは、造血幹細胞研究の大きな課題の一つであった。しかしながら、造血幹細胞の数が非常に少なく、単離の難易度が高かったことから、これまで詳細な解析が困難であった。
これまで、Lineage-c-kit+Sca-1+Flk2-CD34-/lowCD150+を示す造血幹細胞(HSC)群の中に、生涯に渡って自己複製能を有する長期造血幹細胞(LT-HSC)と、一過的な自己複製能しか有さない短期造血幹細胞(ST-HSC)が混在していることが長らく実験的に示唆されていたが、宮西らはこの2つの細胞群をHoxb5の発現の有無で分離できることを明らかにしてきた*1。それでは、幹細胞にとって非常に重要な「自己複製能の有無」を司っているメカニズムはどんなものなのだろうか。従来、LT-HSC(Hoxb5陽性)が長期的に自己複製能を維持できるのは、細胞分裂をほとんど行っていないからだろうと考えられていた。しかしながら、LT-HSCおよびST-HSC(Hoxb5陰性)をそれぞれ単離し細胞周期を解析したところ、両者の間に大きな差異はなかった。EdU取り込み実験の結果は、LT-HSCもST-HSCもほとんど全ての細胞が細胞分裂を行っていることを示していた。また、発現している遺伝子についても、LT-HSCとST-HSCの間には大きな差はなかった。つまり、細胞分裂しないので自己複製能を失わない、ということではないらしい。
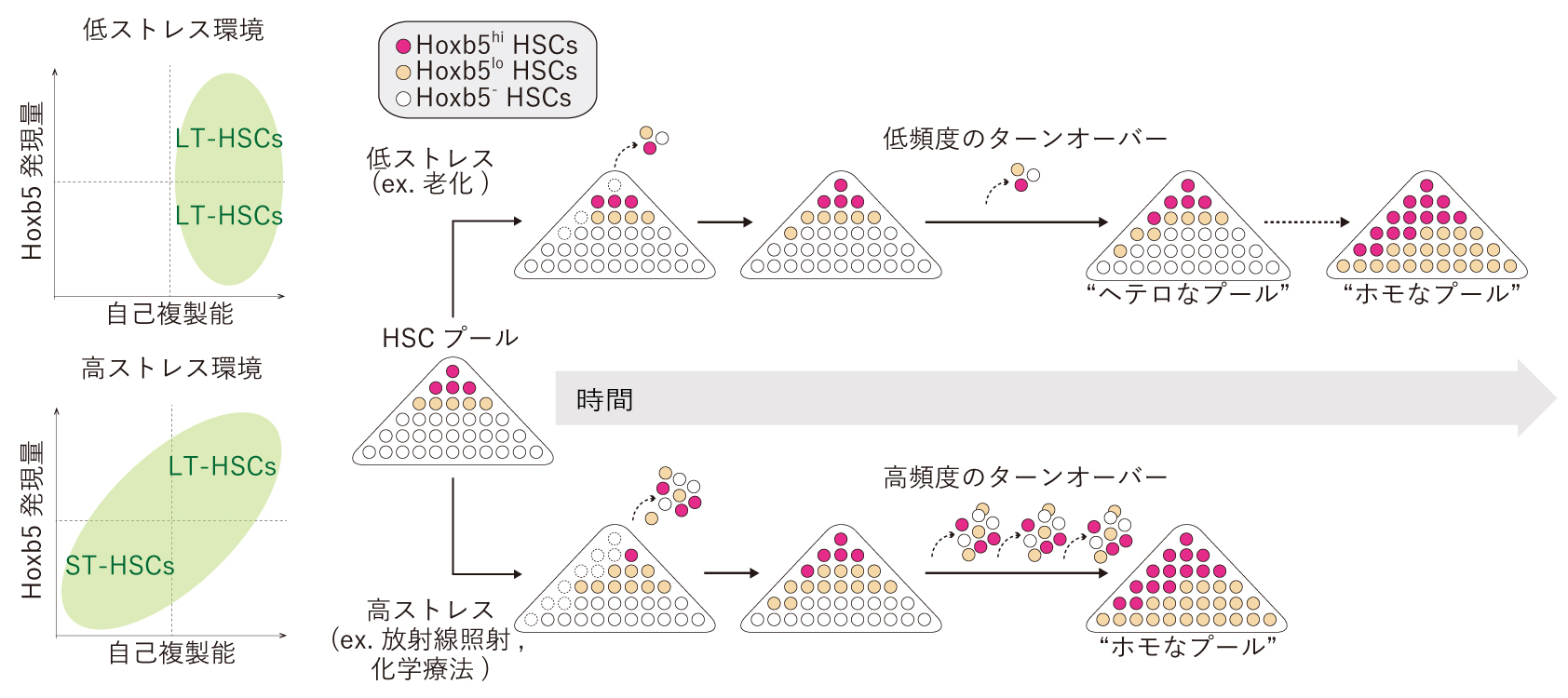
図2.今回の結果から考えられるHSCプールのストレスモデル。ST-HSCは細胞分裂時に分化してしまう確率が
やや高いために、ターンオーバーが繰り返されるとLT-HSCの割合が高まってしまう。
興味深いことに、若齢マウスの骨髄内のHSC分画内におけるLT-HSCとST-HSCの比率は、平常時には2:8程度で安定している。血球系の細胞を全て放射線照射によって死滅させたマウスに、LT-HSCを移植すると、LT-HSCが活発に分裂して増血が回復し、移植細胞に由来する血液細胞が出現する。この時、骨髄内では造血幹細胞分画内の大半のHSCがHoxb5陽性であった。すなわち、放射線照射後の急激な造血回復のために活発な細胞分裂が行われると、LT-HSCとST-HSCのホメオスタシスが崩壊し、LT-HSCの割合が高くなってしまうのだ。事実、HSCと同時に大量の骨髄細胞を移植し、造血回復に必要な細胞分裂を軽減させると、Hoxb5陰性のST-HSCも長期的に自己複製能を維持していた(図1)。以上のことから、LT-HSCとST-HSCにおいて自己複製能を維持できる期間はそれぞれの細胞にもともと規定されているものではなく、細胞分裂というストレスが高い状況でも分化せずに自己複製能を維持できるかどうかによって決まるのではないかと示唆された。さらに、ST-HSCにHoxb5を強制発現させると細胞分裂の頻度は変化しないのに自己複製能が長期的に維持されるようになったことから、自己複製能の長期的な維持にHoxb5が重要な役割を担っていることが示された。
「Hoxb5の発現の有無は、HSCが細胞分裂を行う時に分化せずに自己複製を行う確率を規定しているのではないかと考えています。Hoxb5が発現していれば分化せずに自己複製を行う確率が高く、Hoxb5がない場合にはHoxb5を発現しているときと比較してやや分化してしまう確率が高いがために、結果的に自己複製能を長期的に維持することが難しいのだと思います。」と宮西研究リーダーは語る。「HSC内でLT-HSCとST-HSCの割合が維持されることは、ライフサイクルを通じて個体の造血系のホメオスタシスを維持するために非常に重要なのだと思います。このホメオスタシスが破綻してLT-HSCが濃縮してしまった時に、健康や寿命に対してどのような表現型が現れるのかについては、今後も解析を続けていきたいと思っています。」
高橋 涼香(BDR・広報グループ)
関連リンク
掲載された論文
参考文献





