チームリーダー
西村 隆史
Ph.D.
成長シグナル研究チーム
[2019年6月 終了]
*現在の連絡先:t-nishimura[at]gunma-u.ac.jp
[at]を@に変えてください
多くの多細胞生物は、発育成長過程において器官や体の大きさが遺伝学的に決められています。その一方で、細胞の増殖や組織の形成は、温度や栄養源という外部環境により影響を受けます。各組織の大きさは何らかのメカニズムで認識され、組織自身の増殖が制御され、また成長過程における成熟タイミングとして個体に反映されます。当研究チームでは、ショウジョウバエおよび哺乳類培養細胞を用いて、栄養源認識システムと細胞間シグナルの実体について、統合的な理解を目指しています。

研究テーマ
- 成長過程における個体サイズの調節機構
- 発育成長タイミングの制御機構
- 栄養源認識の分子機
主要論文
Sasaki A, Nishimura T, Takano T, et al.
white regulates proliferative homeostasis of intestinal stem cells during aging in Drosophila
Nature Metabolism doi: 10.1038/s42255-021-00375-x
Yamada T, Hironaka KI, Habara O, et al.
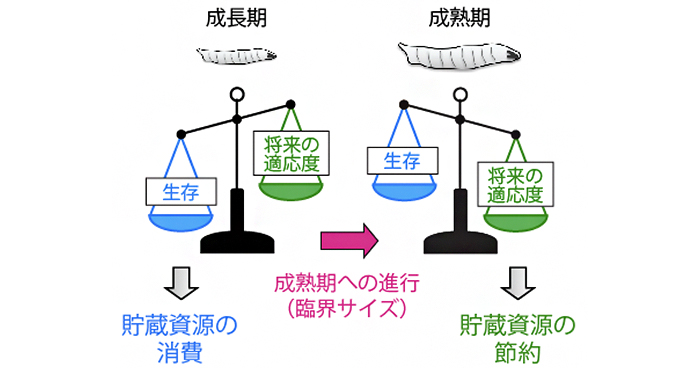
A developmental checkpoint directs metabolic remodeling as a strategy against starvation in Drosophila.
Nature Metabolism (2020) doi: 10.1038/s42255-020-00293-4
Nishimura T.
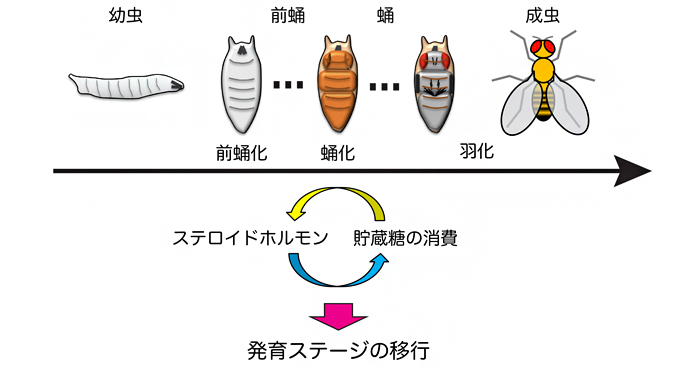
Feed-forward regulation of glucose metabolism by steroid hormones drives a developmental transition in Drosophila.
Current Biology 30(18). 3624-3632 E5 (2020) doi: 10.1016/j.cub.2020.06.043
Imura E, Shimada-Niwa Y, Nishimura T, et al.
The Corazonin-PTTH Neuronal Axis Controls Systemic Body Growth by Regulating Basal Ecdysteroid Biosynthesis in Drosophila melanogaster.
Current Biology 30(11). 2156-2165 E5 (2020) doi: 10.1016/j.cub.2020.03.050
Matsushita R, Nishimura T.
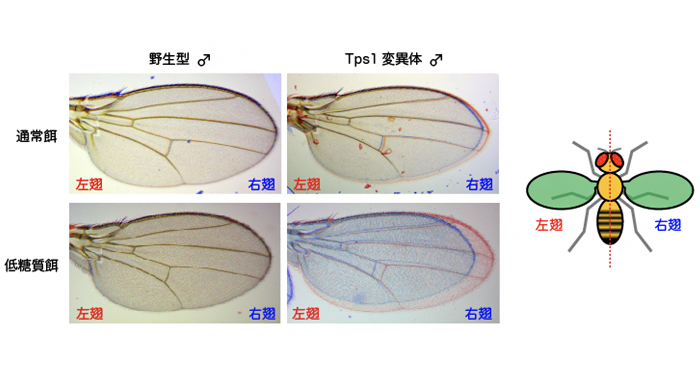
Trehalose metabolism confers developmental robustness and stability in Drosophila by regulating glucose homeostasis
Communications Biology 3. 170 (2020) doi: 10.1038/s42003-020-0889-1
Hironaka K, Fujimoto K, Nishimura T.
Optimal scaling of critical size for metamorphosis in the genus Drosophila.
iScience 20. 348-358 (2019) doi: 10.1016/j.isci.2019.09.033
Yasugi T, Yamada T, and Nishimura T.
Adaptation to dietary conditions by trehalose metabolism in Drosophila.
Scientific Reports 7. 1619 (2017) doi :10.1038/s41598-017-01754-9
Yoshida M, Matsuda H, Kubo H, and Nishimura T.
Molecular characterization of Tps1 and Treh genes in Drosophila and their role in body water homeostasis.
Scientific Reports 6. 30582 (2016) doi:10.1038/srep30582
Okamoto N and Nishimura T.
Signaling from glia and cholinergic neurons controls nutrient-dependent production of an insulin-like peptide for Drosophila body growth.
Developmental Cell 35. 295–310 (2015) doi:10.1016/j.devcel.2015.10.003
Matsuda H, Yamada T, Yoshida M, and Nishimura T.
Flies without trehalose.
Journal of Biological Chemistry 290. 1244–1255 (2015) doi:10.1074/jbc.M114.619411
Okamoto N, Nakamori R, Murai T, et al.
A secreted decoy of InR antagonizes insulin/IGF signaling to restrict body growth in Drosophila.
Genes & Development 27. 87–97 (2013) doi:10.1101/gad.204479.112
Okamoto N, Nishimori Y, and Nishimura T.
Conserved role for the Dachshund protein with Drosophila Pax6 homolog Eyeless in insulin expression.
Proceedings of the National Academy of Sciences of the United States of America 109. 2406–2411 (2012) doi:10.1073/pnas.1116050109