チームディレクター
伊藤 拓宏
Ph.D.
翻訳構造解析研究チーム
[2025年4月よりBDRから生命医科学研究センター(IMS)に所属が変わりました]
拠点横浜
E-mail takuhiro.ito@riken.jp
タンパク質の翻訳は、全ての細胞が持つ最も基本的な機能の一つです。当研究室では、翻訳に関わる分子群の立体構造解析を、主にX線結晶構造解析法とクライオ電子顕微鏡による単粒子解析法を用いて行います。特に複数の真核生物由来の翻訳関連因子やリボソームにより構成される巨大複合体の立体構造解析に重点を置き、複雑な真核生物の翻訳機構の解明を目指します。決定した翻訳関連因子の立体構造を出発点としてそれらに結合する機能性小分子を探索し、タンパク質合成の制御を基とする汎用性の高い薬剤の可能性を探ります。
研究テーマ
- 真核生物の翻訳機構に関する構造生物学
- 生体高分子複合体の結晶化・電子顕微鏡解析に適した試料調製法の開発
主要論文
Iwasaki W, Kashiwagi K, Sakamoto A, et al.
Structural insights into the role of eIF3 in translation mediated by the HCV IRES.
Proceedings of the National Academy of Sciences of the United States of America
122(49), e2505538122 (2025)
doi: 10.1073/pnas.2505538122
Tanaka M, Yokoyama T, Saito H, et al.
Boric acid intercepts 80S ribosome migration from AUG-stop by stabilizing eRF1.
Nature Chemical Biology
20, 605-614 (2024)
doi: 10.1038/s41589-023-01513-0
Matsuura-Suzuki E, Shimazu T, Takahashi M, et al.
METTL18-mediated histidine methylation of RPL3 modulates translation elongation for proteostasis maintenance.
eLife
11, e72780 (2022)
doi: 10.7554/eLife.72780
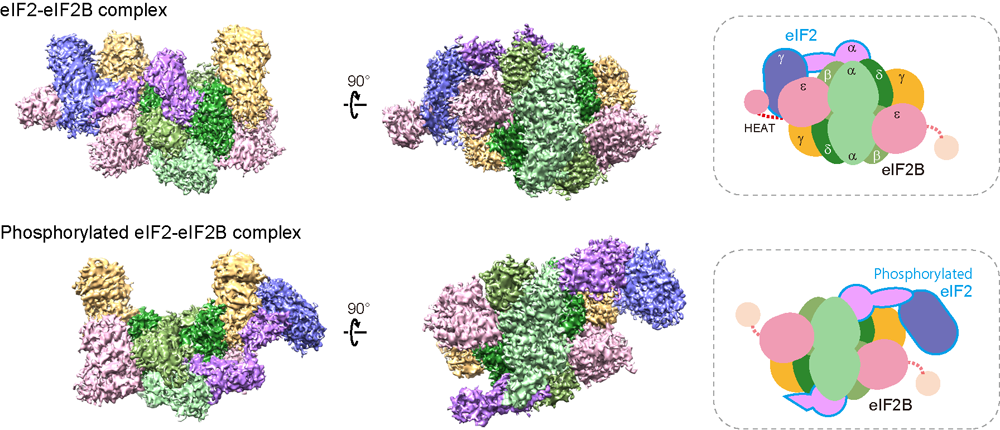
Kashiwagi K, Shichino Y, Osaki T, et al.
eIF2B-capturing viral protein NSs suppresses the integrated stress response.
Nature Communications
12, 7102 (2021)
doi: 10.1038/s41467-021-27337-x
Zyryanova AF, Kashiwagi K, Rato C, et al.
ISRIB blunts the integrated stress response by allosterically antagonising the inhibitory effect of phosphorylated eIF2 on eIF2B.
Molecular Cell
81, 88-103 (2021)
doi: 10.1016/j.molcel.2020.10.031
Yokoyama T, Machida K, Iwasaki W, et al.
HCV IRES Captures an Actively Translating 80S Ribosome.
Molecular Cell
74, 1205-1214 (2019)
doi: 10.1016/j.molcel.2019.04.022
Kashiwagi K, Yokoyama T, Nishimoto M, et al.
Structural basis for eIF2B inhibition in integrated stress response.
Science
364, 495-499 (2019)
doi: 10.1126/science.aaw4104
Iwasaki S, Iwasaki W, Takahashi M, et al.
The translation inhibitor Rocaglamide targets a bimolecular cavity between eIF4A and polypurine RNA.
Molecular Cell
73, 738-748 (2019)
doi: 10.1016/j.molcel.2018.11.026
Kashiwagi K, Takahashi M, Nishimoto M, et al.
Crystal structure of eukaryotic translation initiation factor 2B.
Nature
531, 122-125 (2016)
doi: 10.1038/nature16991
Ito T, Masuda I, Yoshida K, et al.
Structural Basis for methyl-donor-dependent and sequence-specific binding to tRNA substrates by knotted methyltransferase TrmD.
Proceedings of the National Academy of Sciences of the United States of America
112, E4197-E4205 (2015)
doi: 10.1073/pnas.1422981112
Ito T, Yokoyama S.
Two enzymes bound to one transfer RNA assume alternative conformations for consecutive reactions.
Nature
467, 612-616 (2010)
doi: 10.1038/nature09411
Goto-Ito S, Ito T, Kuratani M, et al.
Tertiary structure checkpoint at anticodon loop modification in tRNA functional maturation.
Nature Structural & Molecular Biology
16, 1109-1115 (2009)
doi: 10.1038/nsmb.1653
メンバー

ニュース

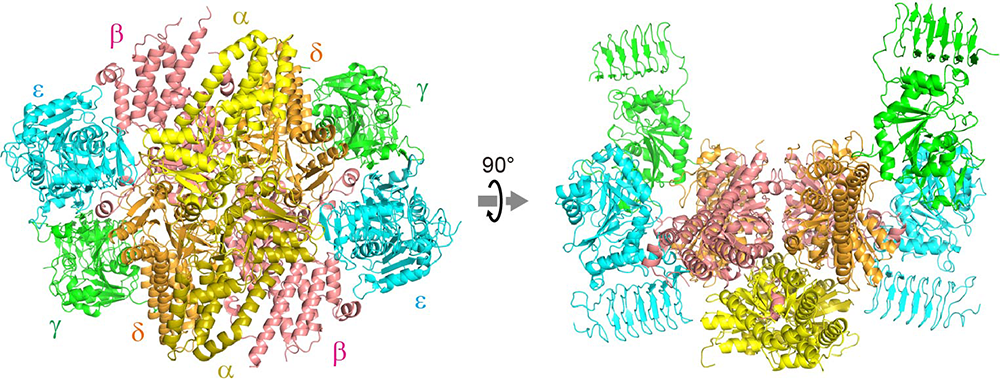
2025年12月5日 研究成果
C型肝炎ウイルスはヒトの翻訳開始因子を巧妙に利用する
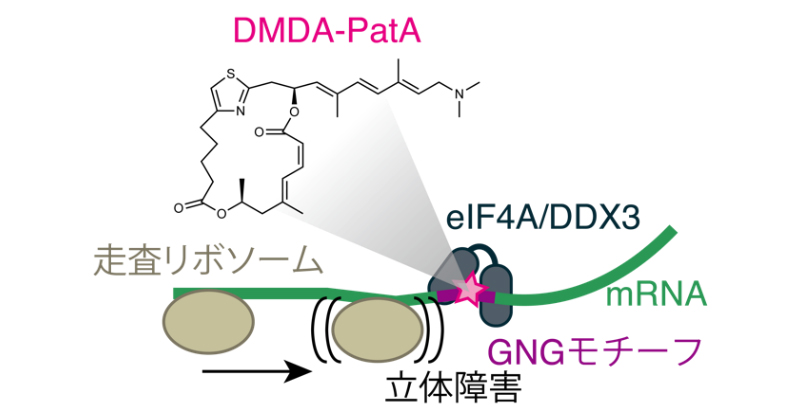
2025年1月10日 研究成果
海産天然物が特定配列のタンパク質合成を阻害

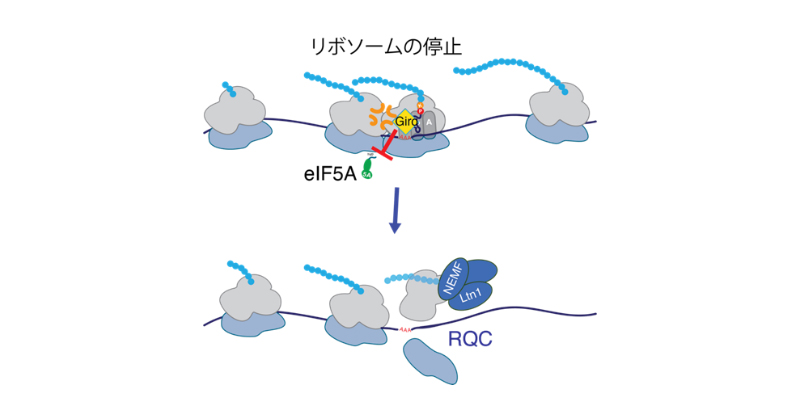
2024年9月13日 研究成果
細胞内の生体分子間のコミュニケーションの仕組みの解明
2024年9月2日 研究成果
狙ったRNAは逃さない!
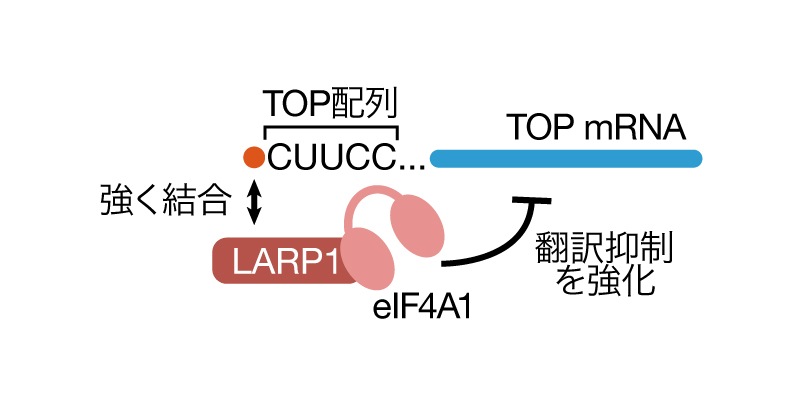
2024年5月21日 研究成果
活性化と阻害のあいだ

2024年5月16日 研究成果
新規ナノ構造体を基盤とするナノ注射器が拓く細胞治療の未来

2024年1月25日 研究成果
植物リボソームの栄養濃度の感知機構を解明

2023年2月28日 研究成果
翻訳阻害剤を介した、植物と糸状菌間の生存競争
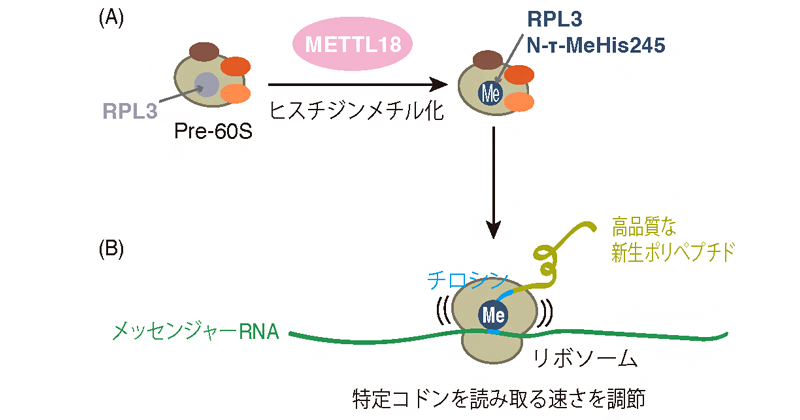
2022年6月21日 研究成果
リボソームタンパク質に起きる翻訳後修飾の機能
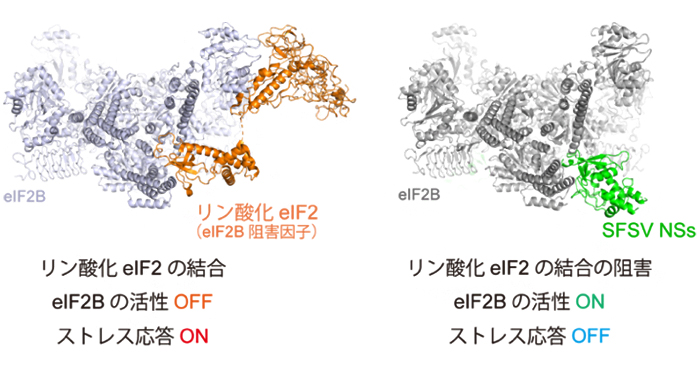
2021年12月7日 研究成果
ウイルスによる細胞のストレス応答抑制機構の解明

2020年12月10日 研究成果
翻訳阻害抗がん剤の二つ目の標的を同定
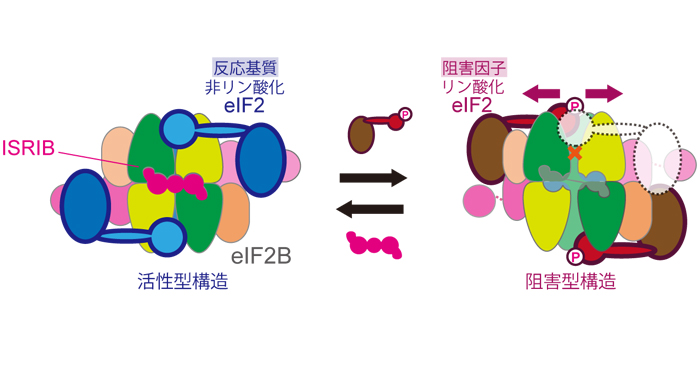
2020年11月21日 研究成果
細胞内ストレス応答を抑える分子の作用機構
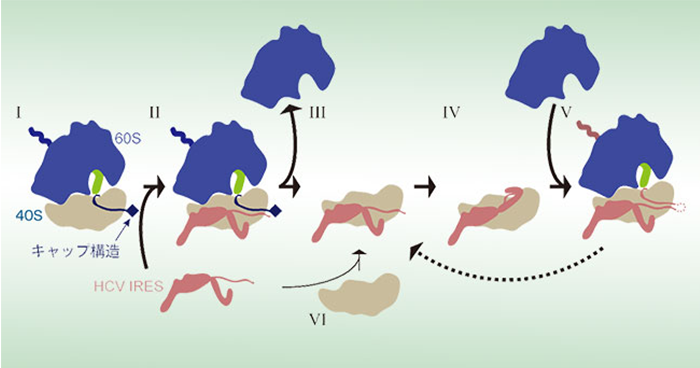
2019年5月14日 研究成果
ウイルスが宿主細胞の翻訳装置を乗っ取る仕組み
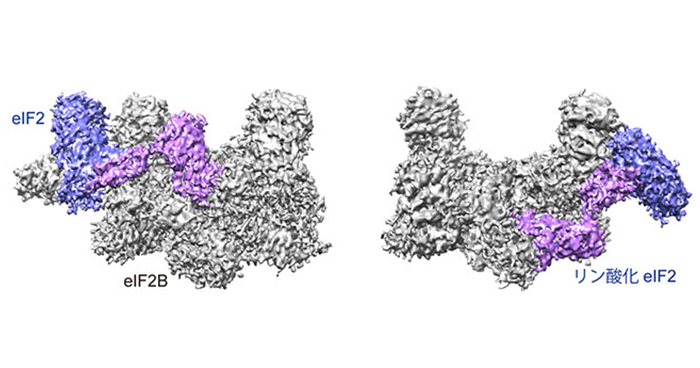
2019年5月3日 研究成果
ストレスでタンパク質合成が止まる仕組み
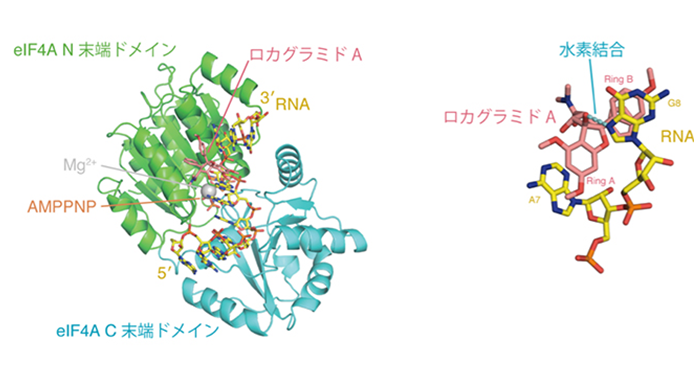
2018年12月28日 研究成果
植物由来抗がん剤の仕組み