
チームリーダー
濱田 博司
M.D., Ph.D.
個体パターニング研究チーム
[2023年3月 終了]
E-mail hiroshi.hamada[at]riken.jp
[at]を@に変えてください
マウスなどの脊椎動物を用いて、体の左右非対称性が生じる仕組みを研究します。とくに、左右対称性を破るために必要な2種類の繊毛(水流を作り出す回転する繊毛と、水流を感知する動かない繊毛)の機能に注目します。また、卵細胞や精子で働くエピジェネテイック因子の個体発生に置ける役割にも注目しています。これらの問題を、遺伝学をベースにしつつ、ライブイメージング・構造生物学・流体工学・数理生物学を取り入れながら、解き明かしたいと思います。
研究テーマ
- 左右対称性を破る繊毛の運動パターンの決定機構
- 不動繊毛が、水流を感知する機構
- 卵子や精子のエピゲノムと個体発生
主要論文
Mizuno K, Shiozawa K, Katoh TA, et al.
Role of Ca2+ transients at the node of the mouse embryo in breaking of left-right symmetry.
Science Advances
6, eaba1195 (2020)
doi: 10.1126/sciadv.aba1195
Kajikawa E, Horo U, Ide T, et al.
Nodal paralogues underlie distinct mechanisms for visceral left-right asymmetry in reptiles and mammals.
Nature Ecology & Evolution
4, 261-269 (2020)
doi: 10.1038/s41559-019-1072-2
Nabeshima R, Nishimura O, Maeda T, et al.
Loss of Fam60a, a Sin3a subunit, results in embryonic lethality and is associated with aberrant methylation at a subset of gene promoters.
eLife
7, e36435 (2018)
doi: 10.7554/eLife.36435
Takaoka K, Nishimura H, Hamada H.
Both Nodal signaling and stochasticity select for prospective distal visceral endoderm in mouse embryos.
Nature Communications
8, 1492 (2017)
doi: 10.1038/s41467-017-01625-x
Minegishi K, Hashimoto M, Ajima R, et al.
A Wnt5 activity asymmetry and intercellular signaling polarize node cells for breaking left-right symmetry in the mouse embryo.
Developmental Cell
40, 439-452 (2017)
doi: 10.1016/j.devcel.2017.02.010
Shinohara K, Chen D, Nishida T, et al.
Absence of radial spokes in mouse node cilia is required for rotational movement but confers ultrastructural instability as a trade-off.
Developmental Cell
35, 236-246 (2015)
doi: 10.1016/j.devcel.2015.10.001
Nakamura T, Saito D, Kawasumi A, et al.
Fluid flow and interlinked feedback loops establish left-right asymmetric decay of Cerl2 mRNA in the mouse embryo.
Nature Communications
3, 1322 (2012)
doi: 10.1038/ncomms2319
Yoshiba S, Shiratori H, Kuo IY, et al.
Cilia at the node of mouse embryos sense fluid flow for left-right determination via Pkd2.
Science (New York, N.Y.)
338(6104), 226-31 (2012)
doi: 10.1126/science.1222538
ニュース
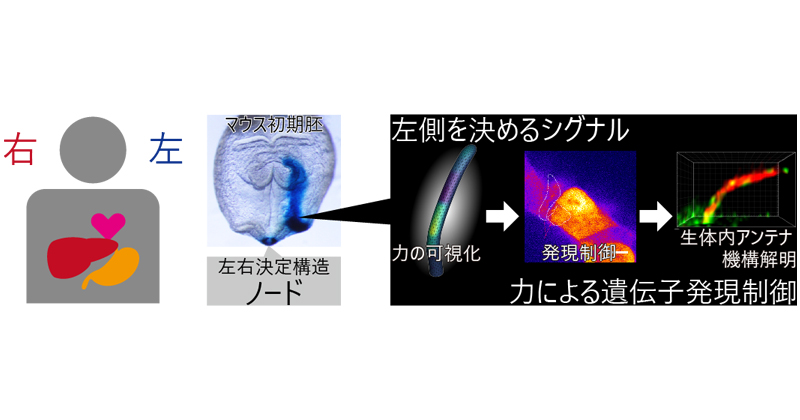
2023年1月12日 研究成果
体づくりの左右非対称性を決める「力」の発見
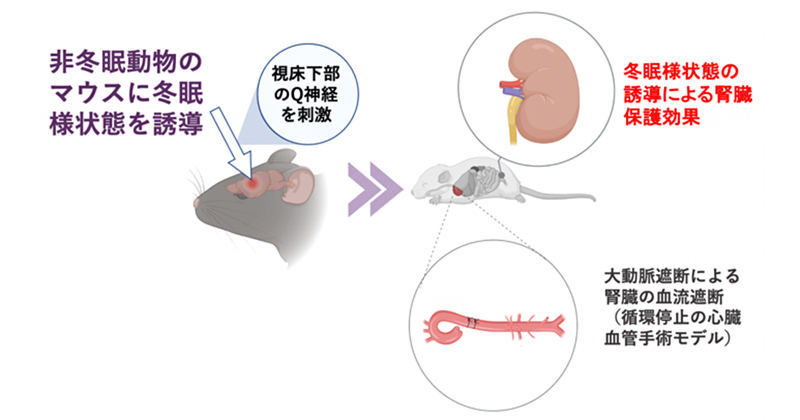
2022年11月14日 研究成果
安全な心臓血管手術のための人工冬眠の可能性

2022年5月11日 BDRニュース
濱田 博司チームリーダーが英国王立協会(The Royal Society)の外国人会員に選出
2021年9月6日 BDRニュース
研究最前線
休眠中の卵胞が目覚める必要条件を発見
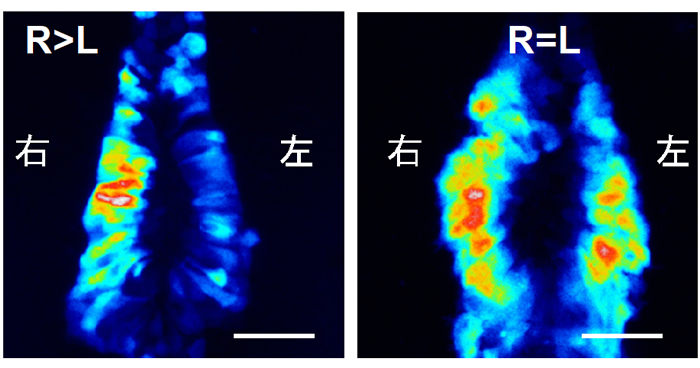
2021年7月30日 研究成果
体の左右非対称性はmRNAの分解から始まる
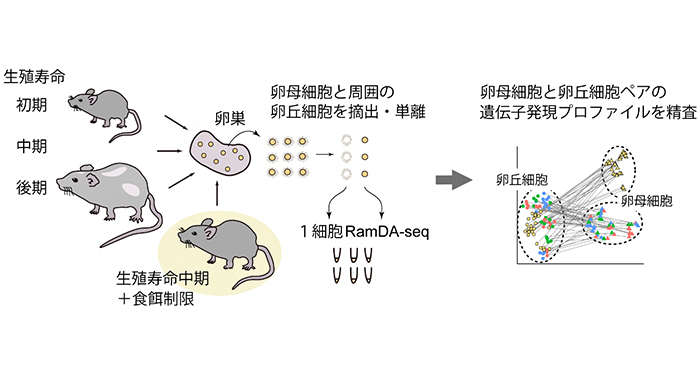
2021年7月13日 研究成果
卵母細胞の老化を1細胞で捉える

2021年6月30日 BDRニュース
濱田 博司 チームリーダーが「高峰記念第一三共賞」を受賞
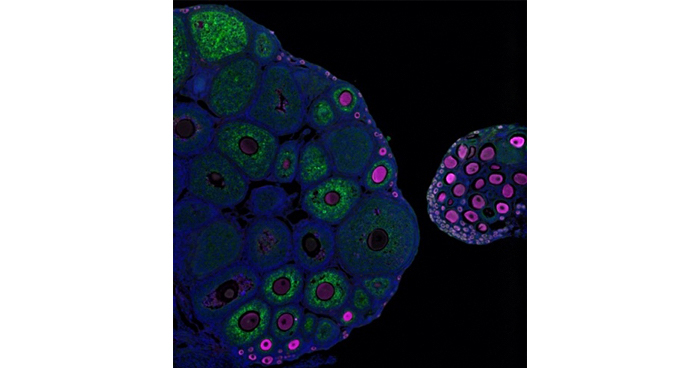
2021年5月28日 研究成果
休眠状態の卵胞が目覚めるためのシグナル

2020年11月11日 BDRニュース
濱田チームリーダーが兵庫県科学賞を受賞
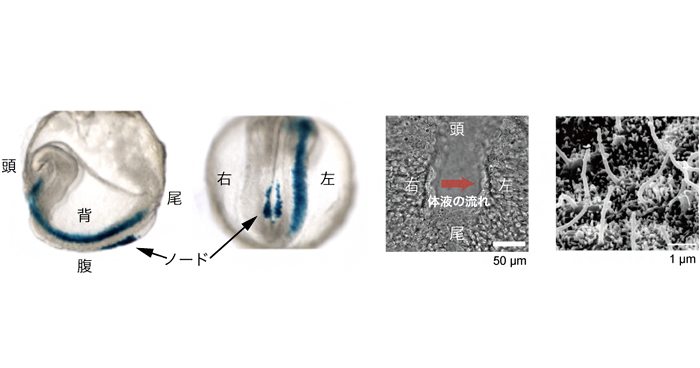
2020年7月28日 研究成果
動物の左右決定に関わるカルシウムイオンの役割

2020年5月7日 BDRニュース
BDRの研究ネホリハホリ
卵子の方が精子より複雑

2020年1月9日 研究成果
哺乳類と鳥類の左右非対称性メカニズムの乖離を説明
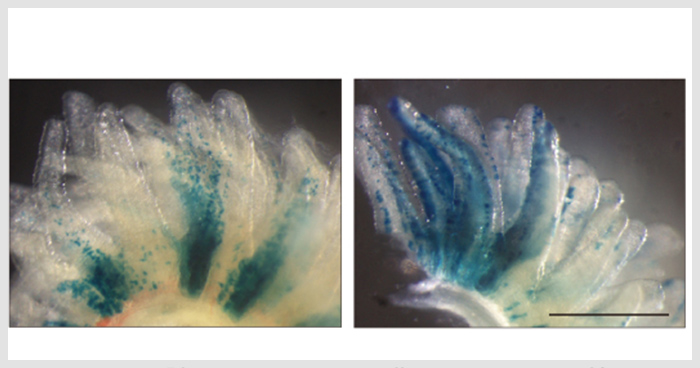
2018年11月1日 研究成果
Fam60aはメチル化を制御して遺伝子発現を変化させる





