臨床グレードのヒトiPS細胞由来心血管系細胞多層体のラットにおける治療効果を確認
2021年11月8日
心臓は心筋という筋肉の細胞の塊である。この力強い筋肉の塊が、一定のリズムで縮んだり戻ったりすることで、全身に血液を送り出すポンプとして機能している。体のいろいろなところで働いている細胞は、血液の循環によって酸素を供給されないと死んでしまう。それは心臓の細胞も同じである。心臓にも血管が張り巡らされており、収縮に必要なエネルギー源を血液から受け取っている。だからこの心臓の血管が詰まって酸素が供給されなくなると、心筋細胞が壊死してしまい、ポンプとしての力を発揮することができなくなる。壊れてしまったポンプ機能を、再生させることはできるだろうか。
理研BDRの升本英利研究リーダー(臨床橋渡しプログラム心疾患iPS細胞治療研究)らの共同研究チーム*1は、心筋梗塞モデルラットに臨床グレードのヒトiPS細胞由来心臓細胞多層体を移植すると、ポンプ機能が回復し、細胞が壊死して固くなった部位の面積が減少するなど、治療効果があることを確認した。本成果は科学誌JTCVS Openに2021年9月30日付で掲載された。
心筋梗塞などに起因する重症の心不全では、心臓のポンプ機能が著しく低下し、全身に十分な血液を送り出すことができなくなる。この重症心不全の治療には心臓移植が有効だが、心臓移植を受けられるまでに平均で3年近く待機を余儀なくされたり、待機している患者のうち20%程度しか移植を受けられないなど、非常に限定的な治療法となっている、また、心臓移植とは別に植込み型の補助人工心臓という選択肢もあるが、心臓移植待機中の患者への植え込みしか保険償還されておらず、植込み手術を行っても術後に不具合が高頻度に発生したりするなど、問題も多い。そのため、再生医療による新たな重症心不全の治療法が選択肢となることが期待されている。
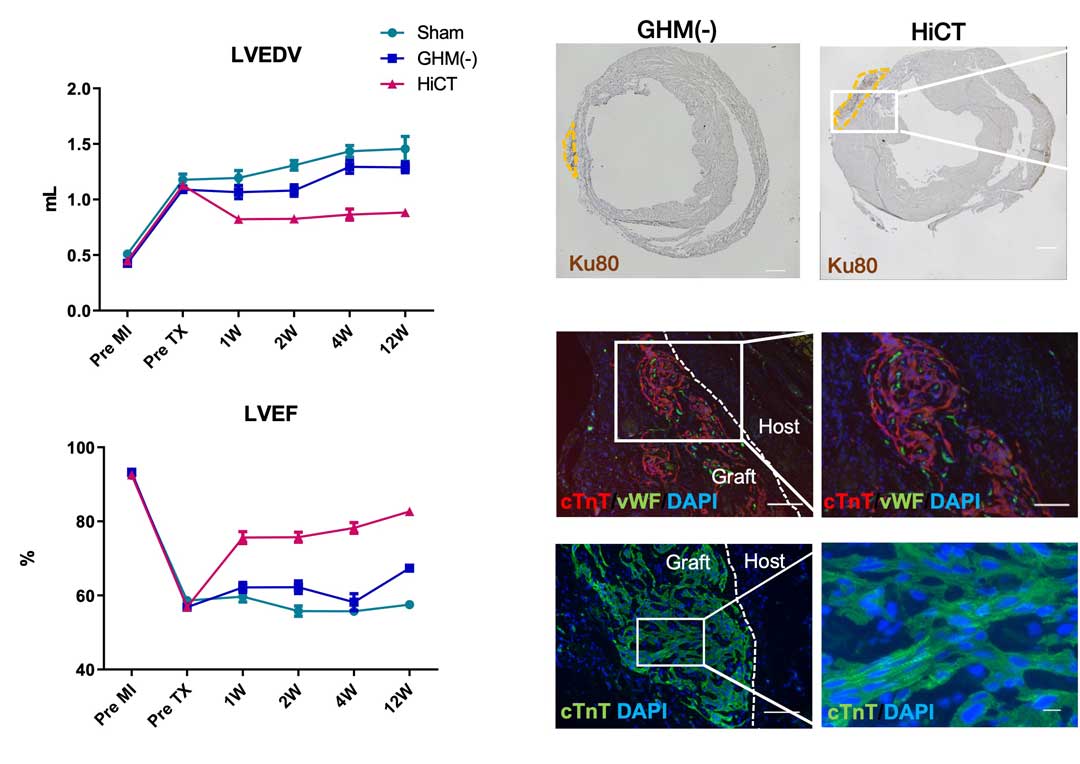
図.心血管系細胞多層体を移植した心筋梗塞モデルラットの心臓機能と組織の変化。(左) 心血管系細胞多層体の移植によって、心筋梗塞後の心臓の肥大が抑えられ(上)、収縮力も回復していた(下)(ピンク:多層体移植)。(右)移植後の組織は定着し(上)、移植片には血管網(中)やサルコメア構造(下)も構成されていた。
升本らは、これまでにマウスES細胞から心筋細胞、血管内皮細胞および血管壁細胞を分化誘導し、温度感受性高分子ポリマーとゼラチンハイドロゲルを用いることで、これらの心血管系細胞を5層積層した心血管系細胞多層体を作製し、ラットへの移植後に生着して機能することを報告してきた。今回、ヒトiPS細胞から作製した心臓組織の移植によってダメージを受けたラットの心臓の機能が回復するかどうかを確認するに当たり、升本らはヒトでの治療を見据えて臨床グレードのヒトiPS細胞を使用した。また、iPS細胞から心筋細胞や血管内皮細胞、血管壁細胞の分化誘導効率を上げるために、従来の方法にWnt阻害剤を添加するプロトコルに改変したところ、心血管細胞の分化誘導効率が改善した。
改善されたプロトコルを用いて、臨床グレードで作成された心血管系細胞多層体を心筋梗塞モデルラットに移植をしたところ、超音波検査およびMRI検査の結果から心筋梗塞後の心臓の肥大が抑えられ、収縮力も回復していた。また心筋梗塞後に心筋が線維化してかさぶた状になると、その部分が固くなって心臓の機能が低下するため、心筋が繊維化する範囲を限定することは心筋梗塞後の心臓機能の回復にとって非常に重要であるが、移植部位を切片にして観察すると、移植した多層体には血管網やサルコメア構造も構成されてラットの心臓組織に生着し、また心筋梗塞後の心臓組織の線維化も多層体の移植による血流の回復によって抑制されていることがわかった。
「心血管系細胞多層体の移植によって、ラットにおける心筋梗塞部位の血管形成が誘導されて心筋組織が再生し、心機能が回復することがわかりました。」と升本研究リーダーは語る。「今後はヒトでの心血管系細胞多層体の移植についての臨床研究に向けて、安全性や治療効果についてさらなる検証を積み重ねていきたいと思います。」
高橋 涼香(BDR・広報グループ)
*1本研究は以下の研究グループの共同研究で実施されました。
長田裕明(京都大学大学院、京都大学iPS細胞研究所)
川東正英(京都大学医学部付属病院、京都大学iPS細胞研究所)
藤田大樹(iHeart Japan株式会社(研究当時))
田畑泰彦(京都大学ウイルス・再生医科学研究所)
湊谷謙司(京都大学医学部付属病院)
山下潤(京都大学iPS細胞研究所)
升本英利(京都大学医学部付属病院、理研BDR)
関連リンク
掲載された論文





