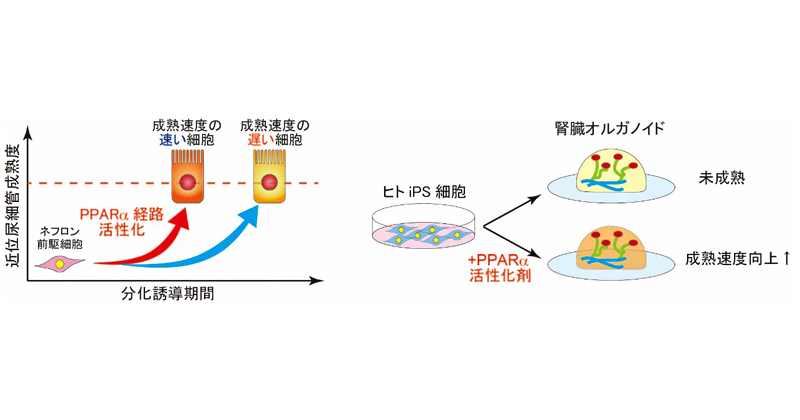
再生医療研究の究極の目標とはなんだろうか。私たちはこの目標を、試験管内でヒト多能性幹細胞を分化誘導し、任意の臓器を完全な形で創り上げる事だと考えています。これまでに私たちはヒト多能性幹細胞から中間中胚葉を分化誘導し、そこから糸球体、尿細管、集合管、血管、間質組織を内包する腎臓オルガノイドを作りました。しかし、サイズ、構造的複雑性、成熟度の点から実際のヒト腎臓と比較すると、腎臓オルガノイドはまだ未完成であると言わざるを得ません。当研究室では、この腎臓オルガノイドの作製系をブラッシュアップし、将来的に移植可能なレベルの3次元腎臓組織を試験管内で構築することを目指すと共に、膀胱など、腎臓と接続するその他の臓器のオルガノイドの作製も行います。また、私たちの持つ、中胚葉・腎臓誘導系から新たな知見を得て、これをヒト発生学へフィードバックすることを目指します。ヒト多能性幹細胞から腎臓細胞までの分化誘導過程にはマウス発生学では説明できない現象もあります。分化誘導過程の細胞の挙動を試験管内で詳しく観察することで、ヒトの中内胚葉系臓器や尿路系臓器の発生メカニズムを解明します。
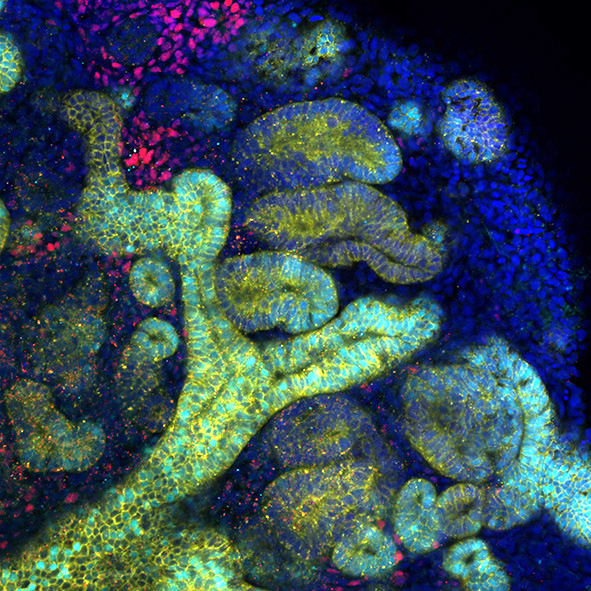
ヒトiPS 細胞から作製した腎臓オルガノイド:ネフロン前駆細胞(赤)と集合管前駆細胞(黄と水色)の両方が存在する。尿細管(黄のみ)も発生している。
腎臓オルガノイドを下から上へと スキャンした動画。集合管(緑と黄)、遠位尿細管(黄のみ)、近位尿細管(赤)、糸球体(緑のみ)の連続した腎構造が確認できる。
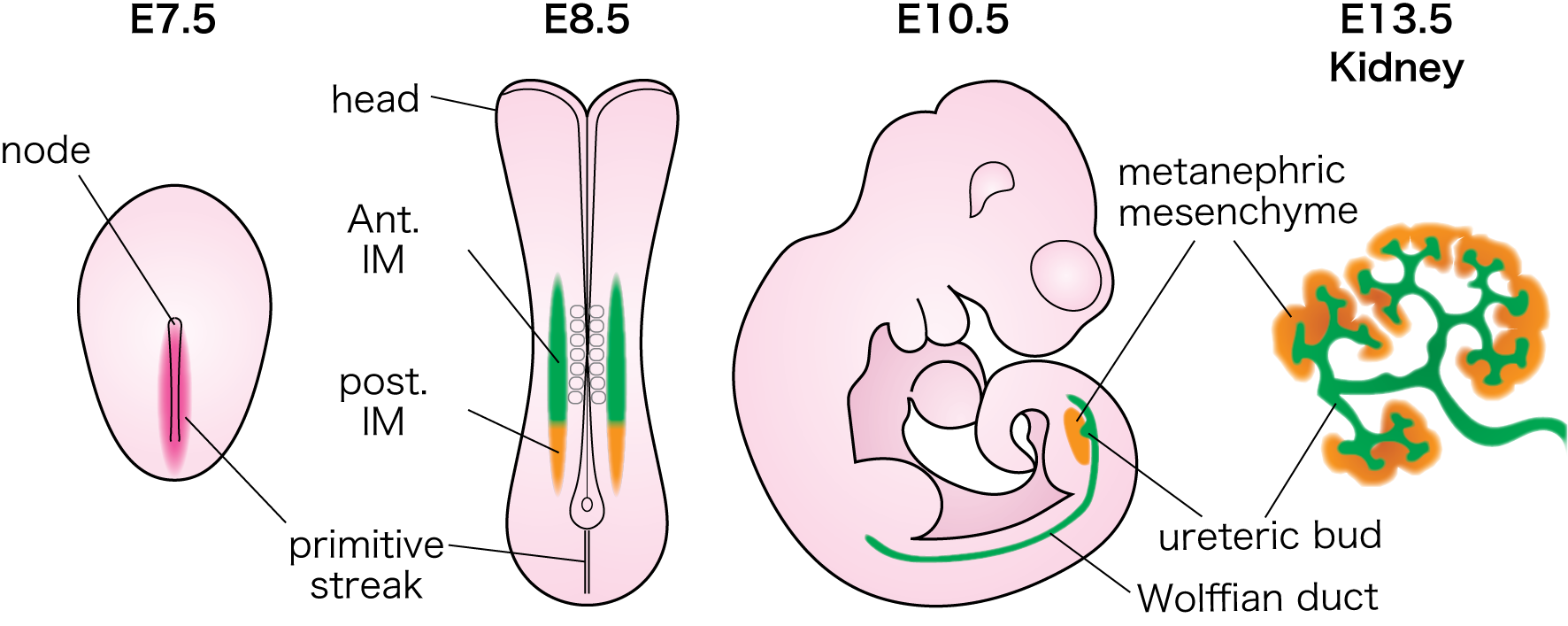
腎臓の発生過程(図はマウス):原始線条は前方および後方中間中胚葉へと分化する。その後、前方はウォルフ管から尿管芽へ、後方は後腎間葉へと分化し、尿管芽と後腎間葉の相互作用により腎臓が発生する。ヒトiPS 細胞を分化させ、この2 つの中間中胚葉を作り分けることができる。
研究テーマ
- 移植可能な尿路系オルガノイドの作製
- ヒト多能性幹細胞から中内胚葉組織への分化制御メカニズムの解明
- オルガノイドをプラットフォームとしたヒト器官発生学
主要論文
Matsubayashi M, Sakaguchi YM, Sahara Y, et al.
27-Hydroxycholesterol regulates human SLC22A12 gene expression through estrogen receptor action.
FASEB Journal
35(1), e21262 (2021)
doi: 10.1096/fj.202002077R
Knarston IM, Pachernegg S, Robevska G, et al.
An In Vitro Differentiation Protocol for Human Embryonic Bipotential Gonad and Testis Cell Development.
Stem Cell Reports
15(6), 1377-1391 (2020)
doi: 10.1016/j.stemcr.2020.10.009
Yamamura T, Horinouchi T, Adachi T, et al.
Development of an exon skipping therapy for X-linked Alport syndrome with truncating variants in COL4A5.
Nature Communications
11(1), 2777 (2020)
doi: 10.1038/s41467-020-16605-x
Takasato M, Wymeersch FJ.
Challenges to future regenerative applications using kidney organoids.
Curr. Opin. Biomed. Eng.
13, 144-151 (2020)
doi: 10.1016/j.cobme.2020.03.003
Takasato M.
Advice for the Next Generation: Minoru Takasato.
Cell Stem Cell
24, 688-689 (2019)
doi: 10.1016/j.stem.2019.04.009
Phipson B, Er PX, Combes AN, et al.
Evaluation of variability in human kidney organoids.
Nature Methods
16(1), 79-87 (2019)
doi: 10.1038/s41592-018-0253-2
van den Berg CW, Ritsma L, Avramut MC, et al.
Renal Subcapsular Transplantation of PSC-Derived Kidney Organoids Induces Neo-vasculogenesis and Significant Glomerular and Tubular Maturation In Vivo.
Stem Cell Reports
10(3), 751-765 (2018)
doi: 10.1016/j.stemcr.2018.01.041
Takasato M, Er P X, Chiu H S, Little M H.
Generation of kidney organoids from human pluripotent stem cells.
Nature Protocols
11, 1681-1692 (2016)
doi: 10.1038/nprot.2016.098
Takasato M, Er P X, Chiu H S, et al.
Kidney organoids from human iPS cells contain multiple lineages and model human nephrogenesis.
Nature
526, 564-568 (2015)
doi: 10.1038/nature15695
Takasato M, Little M H.
The origin of the mammalian kidney: implications for recreating the kidney in vitro.
Development
142, 1937-1947 (2015)
doi: 10.1242/dev.104802
Takasato M, Er P X, Becroft M, et al.
Directing human embryonic stem cell differentiation towards a renal lineage generates a self-organizing kidney.
Nature Cell Biology
16, 118-126 (2014)
doi: 10.1038/ncb2894
メンバー
髙里 実
チームディレクター
趙 薇
研究員
WYMEERSCH Filip Jos
研究員
谷口 純一
基礎科学特別研究員
TRUSH Olena
研究員
佐原 義基
客員研究員
福井 智恵
テクニカルスタッフⅠ
籔内 研佑
リサーチアソシエイト
尾藤 和浩
リサーチアソシエイト
能登 理央
研修生
宇野 亘
大学院生リサーチ・アソシエイト
臼田 ゆかり
研修生
佐藤 敦紀
大学院生リサーチ・アソシエイト
後藤 雅弥
研修生
山下 恵理
事務パートタイマーⅠ